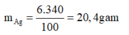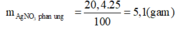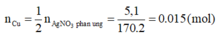Ngâm một vật bằng đồng có khối lượng 5g trong 250 g dung dịch AgNO3 8% chỉ sau một thời gian ngắn Lấy vật ra và kiểm tra thấy khối lượng AgNO3 trong dung dịch bắt đầu giảm 85%
a) tính khối lượng vật lý ra sao Khi lau khô
b) tính nồng độ phần trăm của các chất hòa tan trong dung dịch phản ứng sau khi Lấy vật ra